Lai vadītājā iegūtu un uzturētu elektrisko strāvu, starp vadītāja galiem jānodrošina elektriskais lauks. Šo uzdevumu izpilda strāvas avoti.
Strāvas avoti ir iekārtas, kas izmantojot kādu no enerģijas veidiem, veic elektrisko lādiņu nodalīšanu. Veiktā darba rezultātā viens no elektrodiem uzlādējas negatīvi - elektronu pārpalikums, bet otrs pozitīvi - elektronu iztrūkums.
Līdzstrāvas avoti:
- Voltas stabs - pirmais strāvas avots, ko \(18\). gadsimta beigās izveidoja itālis Alesandro Volta. Voltas elementā vielu ķīmiskā enerģija tiek pārvērsta elektroenerģijā.

Voltas elements sastāvēja no vara (Cu) un cinka (Zn) plāksnītēm, kas bija iegremdētas sērskābes šķīdumā. Ķīmisku reakciju rezultātā cinka plāksnīte kļūst par negatīvo polu, bet vara plāksnīte par pozitīvo polu. Elementa trūkums - nedarbojas ilgstoši.
- galvaniskie elementi - ķīmisku reakciju rezultātā rodas elektriskā enerģija.
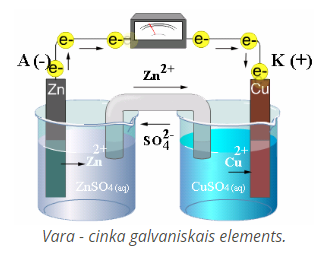
Iegremdējot vara un cinka elektrodus sērskābē, sākas metālu reakcijas ar sērskābi. Varam reaģējot ar sērskābi veidojas vara sulfāts , kas disociē pozitīvajos un negatīvajos jonos. Vara elektrods atdod elektronus un uzlādējas pozitīvi. Cinkam reaģējot ar sērskābi veidojas cinka sulfāts , kas arī disociē pozitīvajos un negatīvajos jonos. Cinka elektrods piesaista elektronus un uzlādējās negatīvi. Ar ķīmisku reakciju palīdzību panākta lādiņu nodalīšana.
1888. gadā vācu pētnieks Gasners izgudroja sauso bateriju, šķidro elektrolītu aizvietodams ar atbilstoša sastāva želeju.
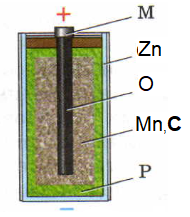
Cilindriskā cinka traukā Zn nostiprināts ogles stienītis O. Stienītis ievietots audekla maisiņā Mn, C, kurš pildīts ar mangāna oksīda un ogles maisījumu. Atlikušo telpu starp maisiņu un korpusu aizpilda ar želejveida pastu P, kas kalpo par elektrolītu.