Skābes ir kodīgas un bīstamas vielas, kas sastāv no ūdeņraža jona (tabulā zemāk zaļā krāsā) un skābes atlikuma (tabulā zemāk dzeltenā
krāsā), kuru var atrast arī skābju, bāzu un sāļu šķīdības tabulā.
Skābes formulu izveidošana
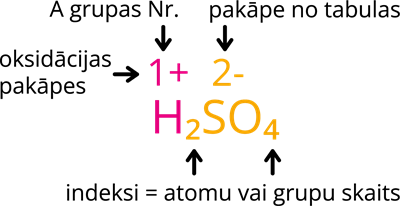
1. darbība: uzraksti oksidācijas pakāpes virs elementiem un skābes atlikuma grupas. Pozitīvā ūdeņraža jona oksidācijas pakāpe sakrīt ar A grupas numuru un tā vienmēr ir 1+, skābes atlikumam oksidācijas pakāpi nosaki pēc sāļu, skābju un hidroksīdu šķīdības tabulas.
2. darbība: indeksus izvieto tāpat kā binārajā savienojumā (savienojumos, kas sastāv no 2 dažādiem elementiem): ūdeņraža jona oksidācijas pakāpi bez "+" zīmes raksti aiz skābes atlikuma, bet skābes atlikuma oksidācijas pakāpi bez "-" zīmes raksti pie ūdeņraža jona. Ja oksidācijas pakāpe ir 1+ vai 1-, tad to var nerakstīt kā indeksu.
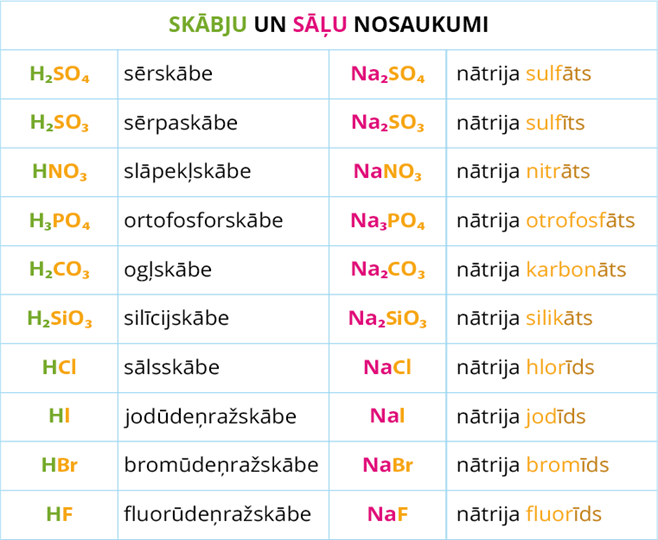
Neorganisko skābju ķīmiskās formulas un nosaukumi:
Tabulā ir redzami arī sāļu nosaukumu piemēri, kurus izmantosi tēmā "Kas ir sāļi?"
Skābju iegūšana
Skābes iegūst skābo (nemetālu) oksīdu reakcijās ar ūdeni. Skābajam oksīdam reaģējot ar ūdeni, veidojas skābe, kas satur ūdeņraža jonu formulas sākumā un skābes atlikumu.
Svarīgi!
Ievēro - skābes atlikums satur tādu ķīmisko element (zemāk tabulā violetā krāsā), kāds ķīmiskais elements ir skābajā oksīdā. Ja reaģē sēra(IV)oksīds, tad izvēlies skābes atlikumu , ja reaģē sēra(VI)oksīds - izvēlies skābes atlikumu .
Reakcijas shēma:
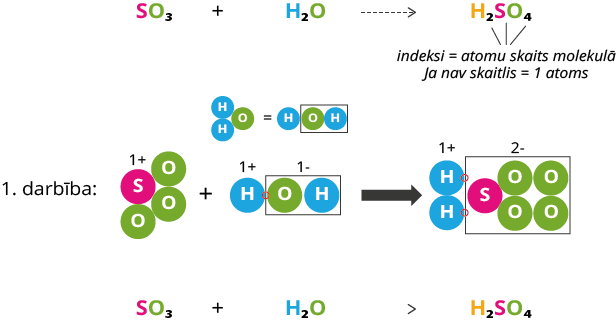
1. darbība: reakcijā redzam, ka no ūdens molekulas izejvielās atšķeļas divi ūdeņraža joni, kas produktos savienojas ar skābo oksīdu, bet oksīdā no izejvielām pievienojas papildus skābekļa atoms no ūdens molekulas un veido skābes atlikumu produktos.
Piemērs:
Skābju izmantošana
Slāpekļskābi lielos daudzumos izlieto minerālmēslu ražošanā. Piemēram, superfosfātu ražošanā. No slāpekļskābes iegūst dažādus nitrātus, ko izmanto galvenokārt par minerālmēsliem. Slāpekļskābi izmanto arī mākslīgo šķiedru, plastmasas un krāsvielu ražošanā.
Sālsskābi plaši izmanto ķīmiskajā rūpniecībā, plastmasu, medikamentu un citu vielu ražošanā, kā arī metālisko virsmu attīrīšanai pirms lodēšanas.