Tu jau zini, ka tīras vielas praktiski nav sastopamas. Dabā, sadzīvē un ražošanā lielāka vielu daļa atrodas kāda maisījuma sastāvā. Atšķirībā no tīrām vielām, maisījumu sastāvs ir mainīgs.
Piemērs:
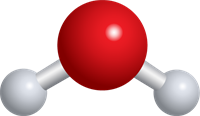
Ūdens molekulā viens skābekļa atoms vienmēr ir saistīts ar diviem ūdeņraža atomiem.
molekulas modeļa attēls.
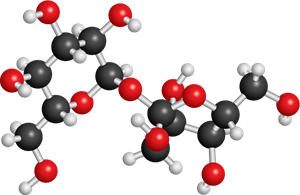
Cukura jeb saharozes molekula sastāv no divpadsmit oglekļa atomiem, divdesmit diviem ūdeņraža atomiem un vienpadsmit skābekļa atomiem.
Saharozes molekulas modeļa attēls.
Pagatavojot cukurūdeni, mēs varam samaisīt saharozi ar ūdeni dažādās proporcijās.
Jebkurai tīrai vielai ir ķīmiskā formula, kas apraksta šīs vielas kvalitatīvo un kvantitatīvo sastāvu, bet maisījumiem tāda formula nepastāv, jo maisījumu sastāvs ir mainīgs. Piemēram, ūdens ķīmiskā formula ir , saharozes ķīmiskā formula ir , bet cukurūdenim, kas var saturēt abas vielas dažādās proporcijās, līdzīgu formulu, kas aprakstītu tā kvantitatīvo sastāvu, izveidot nevar.
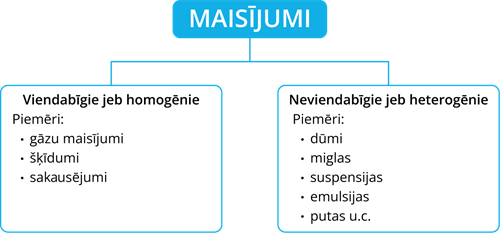
Pēc ārējām pazīmēm maisījumus iedala viendabīgajos jeb homogēnajos un neviendabīgajos jeb heterogēnajos maisījumos. Neviendabīgajos maisījumos pat ar neapbruņoto aci, vai ar mikroskopa palīdzību, var saskatīt dažādas daļiņas vielām, kas ietilpst maisījuma sastāvā, bet viendabīgajos maisījumos atsevišķas daļiņas saskatīt nevar.
Apskatāmo vielu kopu zinātnē ir pieņemts saukt par sistēmu.
MAISĪJUMS = SISTĒMA
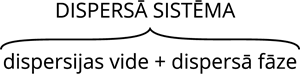
Maisījumus, kuros viena viela ir izkliedēta kādas citas vielas vidē, sauc par dispersām sistēmām (no latīņu dispergere – izkliedēt). Izkliedēto jeb dispergēto vielu sauc par disperso fāzi. Vielu, kurā kādas daļiņas ir izkliedētas, sauc par dispersijas vidi.
Materiālu izstrādāja M. Gorskis