Vienkāršas vielas
Vienkārša viela ir viela, kas sastāv no viena ķīmiskā elementa atomiem.
Bieži vienkāršas vielas sauc tāpat kā attiecīgos ķīmiskos elementus, piemēram, skābeklis apskatāms gan kā noteikts atomu veids, gan viela – kā bezkrāsaina gāze.
Skābeklis ir vienkārša viela, jo sastāv tikai no skābekļa atomiem.
Daudzi ķīmiskie elementi veido vairākas vienkāršās vielas - šo parādību sauc par alotropiju, ogleklis veido ogli, grafītu, dimantu. Šādām vienkāršām vielām mēdz būt savi nosaukumi (ozons, dimants), vai arī tie atvasināti no attiecīgā elementa nosaukuma (pelēkā alva, sarkanais fosfors, monoklīnais sērs).
Fosfora alotropiskie savienojumi:

Svarīgi!
Vienkāršas vielas pamatā iedala metālos un nemetālos,
Svarīgi!
Tipiskākie metāli ir s elementi - sārmu un sārmzemju metāli, kā arī d un f elementi - pārejas metāli, lantanīdi, aktinīdi.
Saliktas vielas
Par saliktām sauc vielas, kas sastāv no vairākiem atomu veidiem.
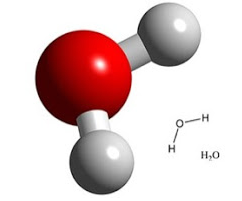
Piemērs:
Ūdens molekula sastāv no 2 ūdeņraža un 1 skābekļa atoma.
Atsauce:
http://www.historyoftheuniverse.com/?p=o2.htm
http://science.widener.edu/
http://lv.wikipedia.org/wiki/Vienk%C4%81r%C5%A1a_viela