Ogļūdeņraži ir organiski savienojumi, kas satur tikai oglekli un ūdeņradi.
Ogļūdeņraži parasti ir nepolāras, ūdenī nešķīstošas vielas. To agregātstāvoklis normālos apstākļos ir atkarīgs no molekulmasas. Ogļūdeņraži ar 4-5 oglekļa atomiem molekulā ir gāzes, 4-5 līdz ~20 oglekļa atomiem molekulā ir šķidrumi, un, ja ir vairāk oglekļa atomu, tad tie ir cietas vielas.
Ogļūdeņražus iedala piesātinātajos (kur visi oglekļa atomi ir hibridizācijā) un nepiesātinātajos (kur daļa vai visi oglekļa atomi ir vai \(sp\) hibridizācijā). Ogļūdeņraži ir galvenā naftas sastāvdaļa.
Ogļūdeņražu iedalījums:

Piesātinātie ogļūdeņraži
- Alkāni
- Cikloalkāni, tos bieži vien apskata kopā ar alkāniem
Nepiesātinātie ogļūdeņraži
- Alkēni
- Alkīni
- Alkadiēni
Arēni jeb aromātiskie ogļūdeņraži
Cikloalkēnus un cikloalkīnus parasti īpaši neizdala un apskata attiecīgi pie alkēniem un alkīniem. Arēni būtībā arī ir nepiesātinātie ogļūdeņraži, taču tiem ir atšķirīgas ķīmiskās īpašības, tāpēc tos nodala atsevišķi.
Alkāni
Alkāni ir piesātināto ogļūdeņražu veids. Piesātinātie ogļūdeņraži ir ogļūdeņraži, kam visi oglekļa atomi ir hibridizācijā, tas ir, tajos nav nepiesātināto saišu, un tāpēc tie neiesaistās pievienošanas reakcijās. Piesātinātos ogļūdeņražus iedala alkānos un cikloalkānos.
Cikloalkānu īpašības būtiski neatšķiras no atbilstošo alkānu īpašībām, tāpēc bieži vien ar jēdzienu piesātinātie ogļūdeņraži saprot tieši alkānus. Alifātiskie (taisnas virknes) ogļūdeņraži ir ķīmiski visai stabili un reaģē visai smagos apstākļos (paaugstinātā temperatūrā). Šos savienojumus var halogenēt, apstarojot ar ultravioleto radiāciju. Cikloalkāni ar lieliem (un nesaspriegtiem) cikliem arī ir stabili. Cikloalkāni ar maziem un saspriegtiem cikliem (ciklopropāns, ciklobutāns) ir ķīmiski aktīvāki. Degviela, kas satur tikai piesātinātos ogļūdeņražus, labāk glabājas (mazāk bojājas uzglabāšanas laikā).
Alkānu vispārīgā ķīmiskā formula ir . Sākot ar \(n = 4\), alkāniem ir iespējami izomēri. Līdz \(n = 4\) alkāni ir gāzes, tālāk ir šķidrumi un cietas vielas.
Alkānu nomenklatūra:
|
Molekulārā formula
|
Nosaukums
|
|
metāns
|
|
|
etāns
|
|
|
propāns
|
|
|
butāns
|
|
|
pentāns
|
|
|
heksāns
|
Vienkāršākie piesātinātie ogļūdeņraži jeb alkāni
|
Ogļūdeņraža nosaukums
|
Struktūrformula
|
Viršanas
temperatūra
|
Agregātstāvoklis
|
|
Metāns
|
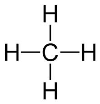 |
-161,6
|
gāze
|
|
Etāns
|
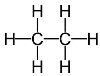 |
-88,6
|
gāze
|
|
Propāns
|
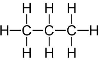 |
-42,1
|
gāze
|
|
Butāns
|
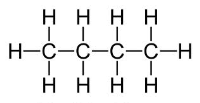 |
-0,5
|
gāze
|
|
Pentāns
|
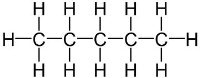 |
+36,07
|
gāze
|
|
Heksāns
|
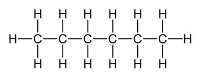 |
+68,7
|
šķidra viela
|
Alkānu fizikālās Īpašības
Ogļūdeņraži, kuru molekulā ir 1-4 oglekļa atomi, parastajos apstākļos ir gāzveida vielas. Tad daži nākamie rindas locekļi ir šķidrumi, bet tālākie - cietas vielas.
Šķidrie, cietie un gāzveida ogļūdeņraži dabā veido vielu maisījumus, ko sauc par naftu un naftas gāzēm. Cieto ogļūdeņražu pārstāvis dabā ir akmeņogles. Cietie ogļūdeņraži ietilpst arī parafīna, vazelīna un dažādu no naftas un akmeņoglēm iegūtu eļļu un smērvielu sastāvā.
Alkānu izmantošana
Piesātināto ogļūdeņražu svarīgāko pārstāvi metānu izmanto gan par kurināmo, gan sintētiskā benzīna ieguvei. Metānu un citus piesātinātos ogļūdeņražus plaši lieto par izejvielām dažādu plastmasu, ķīmisko šķiedru, spirtu, sintētisko kaučuku, mazgāšanas līdzekļu, šķīdinātāju un citu vērtīgu produktu ražošanā. Rūpniecībā no metāna iegūst kvēpus kopēšanas ierīcēm, tipogrāfijas krāsas ražošanai. Kvēpus izmanto arī par pildvielu gumijas ražošanā.
Ogļūdeņražu halogēnatvasinājumus - freonus - dažkārt vēl izmanto ledusskapjos un aerosolos kā gaistošu sastāvdaļu, kaut gan tie ir viens no Zemes ozona slāņa sairšanas cēloņiem.

Attēlā: Propānu - butānu izmanto par kurināmo.