Svarīgi!
Vielas agregātstāvoklis ir atkarīgs no vielas veidojošajām daļiņām, to dabas un savstarpējās mijiedarbības, kā arī temperatūras un spiediena.
Gāzveida stāvoklis
Gāzveida vielām raksturīga tieksme neierobežoti izplesties, spējot aizpildīt jebkuru trauku un ieņemt tā formu. Gāzēm ir arī raksturīgs mainīgs blīvums, jo tas ir atkarīgs no trauka tilpuma, kurā tā atrodas.
Izpētot gāzu īpašības, tika radīta gāzu kinētiskā teorija. Saskaņā ar to gāzes ir molekulu vai atomu kopums, kas vienmēr atrodas kustībā. Molekulas (atomi) kustas ar dažādu ātrumu. Vislielākais vidējais ātrums ir vieglākajām gāzēm. Piemēram, ūdeņraža molekulām vidējais kustības ātrums ir 1698 m/s ( temperatūrā). Citām gāzēm molekulu kustības vidējais ātrums ir aptuveni 300-400 m/s.
Vājās starpmolekulārās mijiedarbības dēļ nelielā spiedienā vai augstā temperatūrā visas tipiskās gāzes izturas apmēram vienādi, tomēr jau parastajā temperatūrā un normālā spiedienā sāk izpausties gāzu individuālās īpašības.
Šķidrs stāvoklis
Šķidrā stāvoklī mijiedarbības spēki starp daļiņām ir pietiekami lieli, lai aizkavētu to haotisko pārvietošanos, bet par mazu, lai pārtrauktu daļu pārvietošanos citai attiecībā pret citu. Nepārtrauktā daļiņu pārvietošanās ir cēlonis šķidrumu stipri izteiktajai pašdifūzijai un tecētspējai.
Ciets stāvoklis
Pētot cietas vielas ar rentgenstariem, konstatēja, ka lielākajai daļai neorganisko vielu kristālrežģa mezglu punktos atrodas atomi un joni, nevis molekulas.
Cietvielas, kam ir raksturīga stingri noteikta daļiņu kārtība, atrodas kristāliskā stāvoklī, toties cietvielas, kurām nav kristāliska uzbūve, atrodas amorfā stāvoklī.
Bieži viena un tā pati viela var atrasties gan kristāliskā, gan amorfā stāvoklī. Vielas amorfais stāvoklis ir nestabilāks par kristālisko stāvokli.
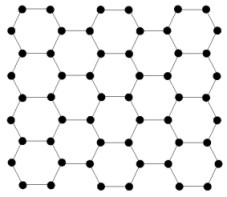 Kristālisks stāvoklis | 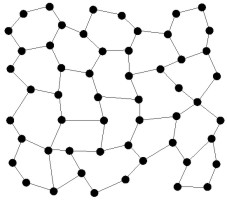 Amorfs stāvoklis |