Pentāns ir tipisks piesātinātais ogļūdeņradis - alkāns. Pentāns normālos apstākļos ir viegls, gaistošs šķidrums. Lieto kā degvielu un šķīdinātāju.

Svarīgi!
Pentānam ir trīs struktūrizomēri ar summāro formulu :
- n-pentāns,
- izopentāns
- neopentāns
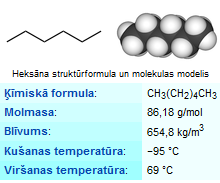
Heksāns pieder pie piesātinātajiem ogļūdeņražiem - alkāniem. Heksāns normālos apstākļos ir viegls, bezkrāsains, gaistošs šķidrums. Lieto kā inertu, nepolāru šķīdinātāju. Iegūst no naftas vieglajām frakcijām.
Svarīgi!
Heksānam ir pieci izomēri:
- n-heksāns
- 2-metilpentāns
- 3-metilpentāns
- 2,3-dimetilbutāns
- 2,2-dimetilbutāns
Etilēns jeb etēns ir bezkrāsaina gāze, tas ir vienkāršākais nepiesātinātais ogļūdeņradis. To iegūst no naftas. To lieto par polietilēna monomēru (polimerizācija), etanola (pievieno ūdeni), vinilhlorīda (hlorēšana) un etilbenzola (pievieno benzolu) izejvielu. Etilēns ir augu hormons un augos piedalās dažādu fizioloģisku un bioķīmisku procesu regulācijā. Piemēram, tas paātrina augļu nogatavošanos.
Etilēnu parasti iegūst no naftas, termiskā krekinga procesā, kur tas ir viens no galvenajiem galaproduktiem. Krekingā lielmolekulāru (relatīvi) piesātinātu ogļūdeņražu maisījumu uzkarsē līdz ~750 - 800 °C un veidojas mazmolekulāri un nepiesātināti ogļūdeņraži. Etilēnu var iegūt arī, dehidratējot etanolu ar koncentrētu sērskābi. Šādā veidā etilēnu iegūst laboratorijā.

Acetilēns ir vienkāršākais alkīns - ogļūdeņradis ar trīskāršo saiti molekulā. Acetilēns ir bezkrāsaina, degoša gāze, kas šķīst acetonā. Acetilēnu var iegūt, kalcija karbīdam reaģējot ar ūdeni, vai arī pirolizējot metānu. Saspiestā un sašķidrinātā veidā acetilēns ir nestabils un var spontāni sadalīties, tāpēc to uzglabā, izšķīdinātu acetonā, vai arī iegūst uz vietas. Acetilēnu lieto metināšanai un metālapstrādei (dzelzs virsmas cietināšanai). Acetilēnu agrāk lietoja arī par ķīmisko izejvielu, taču šādiem mērķiem mūsdienās vairāk lieto naftas ogļūdeņražus, jo tie ir lētāki.
