Vairums no pašreiz zināmajiem 118 ķīmiskajiem elementiem ir metāliskie elementi, kuri veido vienkāršas vielas ar metāliskām īpašībām. Šīs vienkāršās vielas sauc par metāliem.
No metāliem un to sakausējumiem izgatavo daudzas detaļas transportlīdzekļos - vilcienos, automobiļos, tramvajos, trolejbusos, kuģos un lidmašīnās. Bez alumīnija un vara vadiem būtu grūti pārvadīt elektrisko enerģiju. Arī celtniecībā metāla konstrukcijas ieņem ļoti svarīgu vietu. Bez mašīnām un iekārtām, kuras izgatavotas no metāliem un to sakausējumiem, mūsdienās būtu grūti iedomāties lauksaimniecību un rūpniecību. Arī sadzīvē ir daudz metāla izstrādājumu, kuri nepieciešami ikdienā.
Metāli dabā
Neaktīvie metāliskie elementi - varš, sudrabs, zelts - dabā nelielos daudzumos ir sastopami vienkāršu vielu veidā - tīrradņos metāla veidā. Atsevišķos gadījumos dzelzi un dažus citus metālus var atrast arī meteorītu šķembās.
Vidēji aktīvie metāliskie elementi dabā izplatīti galvenokārt rūdu veidā - piemēram, dzelzs dabā ir sastopams rūdu veidā.
Aktīvie metāliskie elementi dabā sastopami galvenokārt sāļu veidā, kas sastopami gan dažādās iegulās, gan izšķīdušā veidā sālsezeru, jūru un okeānu ūdenī.
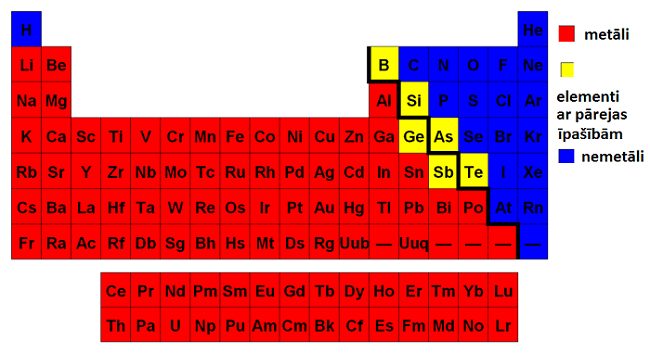
Metāli tabulā atzīmēti sarkanā krāsā.
Svarīgākie metālu iegūšanas paņēmieni:
- No oksīdiem, izmantojot ogli, tvana gāzi \(\mathrm{CO}\) vai ūdeņradi:
- Sulfīdus vispirms apdedzina:
Pēc tam karsē kopā ar ogli:
- No izkausētiem sāļiem, izmantojot līdzstrāvu: