Mazgāšanas līdzekļi
Mazgāšanas līdzekļi ir vielas, kuru šķīdumi spēj atraut netīrumus no mazgājamās virsmas un saistīt tos.
- samazināt ūdens virsmas spraigumu, lai mazgāšanas šķidrums slapinātu virsmu;
- atdalīt netīrumus no virsmas;
- uzturēt netīrumus suspendētā veidā, lai to daļiņas nesaliptu un tās būtu iespējams atdalīt no virsmas.
Ziepes
Ziepju iegūšana
1) Esteru hidrolīze
Piemērs:
Hidrolizējot propionskābes etilesteri nātrija hidroksīda klātbūtnē, veidojas nātrija propionāts (ziepes) un etanols:
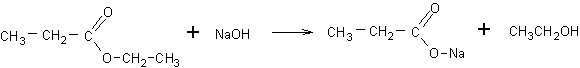
Piemērs:
Hidrolizējot stearīnskābi nātrija hidroksīda klātbūtnē, veidojas nātrija stearāts (ziepes) un ūdens:

3) Tauku hidrolīze
Piemērs:
Hidrolizējot palmitīnskābes triglicerīdu nātrija hidroksīda klātbūtnē, veidojas glicerīns (trīsvērtīgs spirts) un nātrija palmiāts (ziepes):
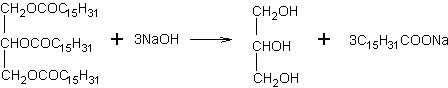
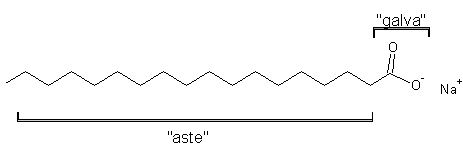
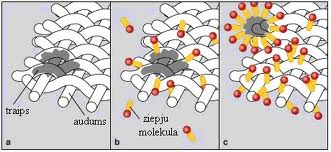
Ziepju molekulām ir divejāda daba. Ziepju molekulas "galvai" ir jonu īpašības un tā viegli šķīst ūdenī, bet garajai "astei" (ogļūdeņraža atlikumam) piemīt spēja šķīst eļļā (taukos). Uzbrūkot netīrumiem, ziepju molekula izmanto savu divejādo dabu. Ziepju molekulas "aste" šķīst eļļā un sašķeļ eļļas pilienu mazākos pilieniņos, kas disperģē šķidrumā. Šos pilieniņus apņem hidratētas ziepju molekulas, neļaujot tiem apvienoties. Ziepju molekulu adsorbcijas dēļ starp virsmu un netīrumu daļiņām sāk darboties atgrūšanās spēki, kas nodrošina daļiņu atdalīšanos no virsmas.
Ziepju trūkumi
Ziepes zaudē savas mazgājošās īpašības cietā un skābā ūdenī.
Cietā ūdenī ir un joni. Ziepes reaģē ar šiem joniem un veido karbonskābju sāļus, kas nešķīst ūdenī. Tāpēc daļa ziepju tiek patērēta šo jonu nogulsnēšanai
Skābā ūdenī ir joni. Ziepes ar šiem joniem stājas apmaiņas reakcijā, izgulsnējot karbonskābi.
Sintētiskie mazgāšanas līdzekļi
Pēc uzbūves sintētiskie mazgāšanas līdzekļi (SML) ir līdzīgi ziepēm. To molekulās ir gara ogļūdeņražu virkne - hidrofobā grupa un jonu tipa "galva" - hidrofīlā grupa.
Mazgājošās vielas - virsmaktīvās vielas sintētiski iegūst galvenokārt no ogļūdeņražiem (naftas pārstrādes produktiem), sērskābes un sodas. Ir vairākas sintētisko virsmaktīvo vielu grupas.
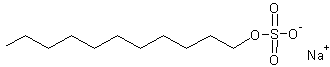
Anjonu virsmaktīvās vielas. Šādi savienojumi visvairāk līdzīgi ziepēm pēc uzbūves un salīdzinoši visvairāk tiek ražoti. Anjonu tipa SML hidrofilo daļu veido sulfātjoni, sulfonātjoni, hidroksīdjoni, bet hidrofobo daļu - dažādu ogļūdeņražu atlikumi. Anjonu virsmaktīvās vielas satur šampūni.
Mazgājošās vielas - virsmaktīvās vielas sintētiski iegūst galvenokārt no ogļūdeņražiem (naftas pārstrādes produktiem), sērskābes un sodas. Ir vairākas sintētisko virsmaktīvo vielu grupas.
Anjonu virsmaktīvās vielas. Šādi savienojumi visvairāk līdzīgi ziepēm pēc uzbūves un salīdzinoši visvairāk tiek ražoti. Anjonu tipa SML hidrofilo daļu veido sulfātjoni, sulfonātjoni, hidroksīdjoni, bet hidrofobo daļu - dažādu ogļūdeņražu atlikumi. Anjonu virsmaktīvās vielas satur šampūni.
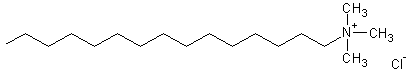
Katjonu virsmaktīvās vielas. Tām ir sliktākas mazgājošās īpašības nekā anjonu virsmaktīvajām vielām, taču piemīt bakteriocīdas īpašības. Lieto dezinfekcijai un tīrīšanai pārtikas rūpniecībā.
Nejonu virsmaktīvās vielas. Tās neveido sāļus ar , vai joniem, nereaģē ar skābēm un pat nelielos daudzumos uzrāda mazgājošas īpašības. Izmanto trauku mazgāšanas līdzekļos.


