Dispersās sistēmas
Vielas sastāv no sīkām daļiņām, un katrai no tām piemīt šīs vielas īpašības. Tīra viela nesatur citu vielu piemaisījumus.
Dabā visas vielas pārsvarā sastopamas maisījumu veidā. Gaiss, ko elpojam, ūdens un pārtikas produkti, ko lietojam uzturā, ieži, kas veido Zemes garozu, ir vairāku tīru vielu maisījumi.
Lai sīkāk izpētītu maisījumu īpašības, zinātnieki maisījumus apskata kā dispersās sistēmas. Nosaukums cēlies no latīņu valodas vārda dispergere, kas nozīmē 'izklīdināt'. Tātad termins dispersā sistēma nozīmē: salikts kopā no izklīdinātām daļām.
Dispersā sistēma sastāv no dispersijas vides un dispersijas fāzes.
Dispersijas vide ir tīra viela vai vielu maisījums, kurā izkliedējas sīki sasmalcinātas citas vielas daļiņas.
Dispersā fāze ir sīki sasmalcināta viela, kura izklīdināta dispersijas vidē.
Dispersā sistēma sastāv no gāzes, šķidruma vai cietas vielas, kurā izkliedētas citas vielas daļiņas.
Disperso sistēmu iedalījums
Dispersās sistēmas pēc izkliedēto daļiņu izmēriem var iedalīt trīs grupās.
- Suspensijas, emulsijas, aerosoli (rupji dispersās sistēmas), kurās daļiņu izmērs ir lielāks par 100 nm.
- Koloidālie šķīdumi, kuros daļiņu izmērs ir no 100 nm līdz 1 nm.
- Īstie šķīdumi, kuros ir atsevišķi izkliedētas molekulas un joni, kuru izmērs ir mazāks par 1 nm.

Dispersās sistēmas var iedalīt arī pēc vides agregātstāvokļa (ciets, šķidrs un gāzveida). Pavisam izšķir deviņus disperso sistēmu tipus.
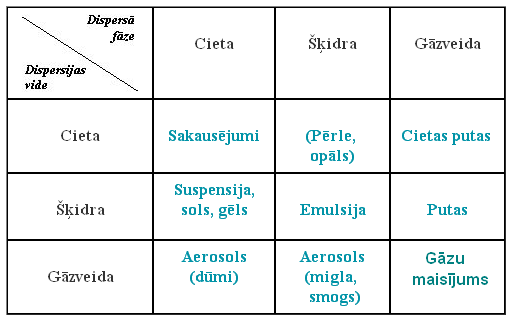

Rupji dispersās sistēmas
Ja šķidrumā ir izkliedētas cietu vielu daļiņas, tad tādu dispersu sistēmu sauc par suspensiju. Suspensijas piemērs ir ūdenī saduļķots māls. Šajā gadījumā ūdens ir dispersijas vide, bet māla daļiņas ir dispersā fāze.
Ja šķidrā vielā ir izkliedētas citu šķidru vielu daļiņas, tad maisījumu sauc par emulsiju. Piemēram, ikdienā bieži lietojama emulsija ir piens, kur šķidrumā ir izkliedētas šķidro tauku daļiņas.
Lai emulsija būtu stabila un nenoslāņotos divos atsevišķos šķidrumos, ir vajadzīgs trešais komponents - emulgators.
Emulgators ir viela, kas palielina spēju eļļai un ūdenim vienam otru slapināt. Pārtikas un kosmētikas rūpniecībā kā emulgatorus izmanto ķīmiskus savienojumus. Pārtikas tehnologi katram produktam rūpīgi izvēlas atbilstošu emulgatoru, lai emulsija pēc iespējas ilgāk nenoslāņotos.
Ja gāzveida vielā ir izkliedētas cietu vai šķidru vielu daļiņas, tad maisījumu sauc par aerosolu. Dūmi ir cietu vielu daļiņu aerosoli, un migla ir šķidru daļiņu aerosols.
Koloidālie šķīdumi
Īstie šķīdumi
Īstajos šķīdumos izkliedētā viela ir sasmalcināta līdz atsevišķām molekulām vai joniem. Parasti vārdu "īsts" nelieto un ar vārdu "šķīdums" saprot tikai tās dispersās sistēmas, kurās izkliedētās vielas ir molekulu vai jonu veidā.
Gan koloidālie šķīdumi, gan īstie šķīdumi ir caurspīdīgi. Tomēr šos šķīdumus var atšķirt, ja caur tiem laiž šauru gaismas kūli. Koloidālā šķīdumā būs novērojams izteikts gaišs konuss. Šādu parādību sauc par Tindala efektu. Ar šī eksperimenta palīdzību var atšķirt koloidālus šķīdumus no īstiem šķīdumiem, kuros Tindala efektu nevar novērot.

Ne koloidālie, ne īstie šķīdumi paši no sevis nesadalās sastāvdaļās. Koloīdās daļiņas gan var salipt lielākās daļiņās. Šo procesu sauc par koagulāciju. Koagulāciju var izraisīt, ja šķīdumu karsē vai ievada tajā lielu daudzumu jonu. Koagulācijas norisē radušās lielākās daļiņas izveido suspensiju un pēc tam pamazām nosēžas.